Асептическое производство медицинской продукции. Часть 1. Общие требования
На нашем сайте можно бесплатно скачать Руководящий документ ГОСТ Р ИСО 13408-1-2000 в удобном формате. Узнать актуальный статус документа «Асептическое производство медицинской продукции. Часть 1. Общие требования» на 2016 год.
Скрыть дополнительную информацию

Страница 1

Страница 2

Страница 3

Страница 4

Страница 5

Страница 6

Страница 7

Страница 8

Страница 9

Страница 10

Страница 11

Страница 12

Страница 13

Страница 14
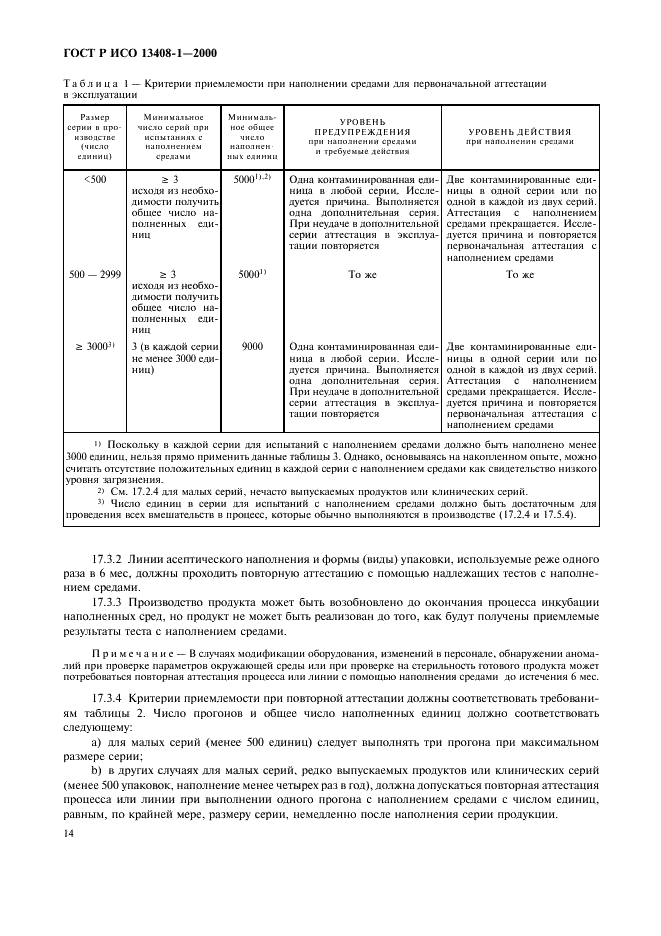
Страница 15
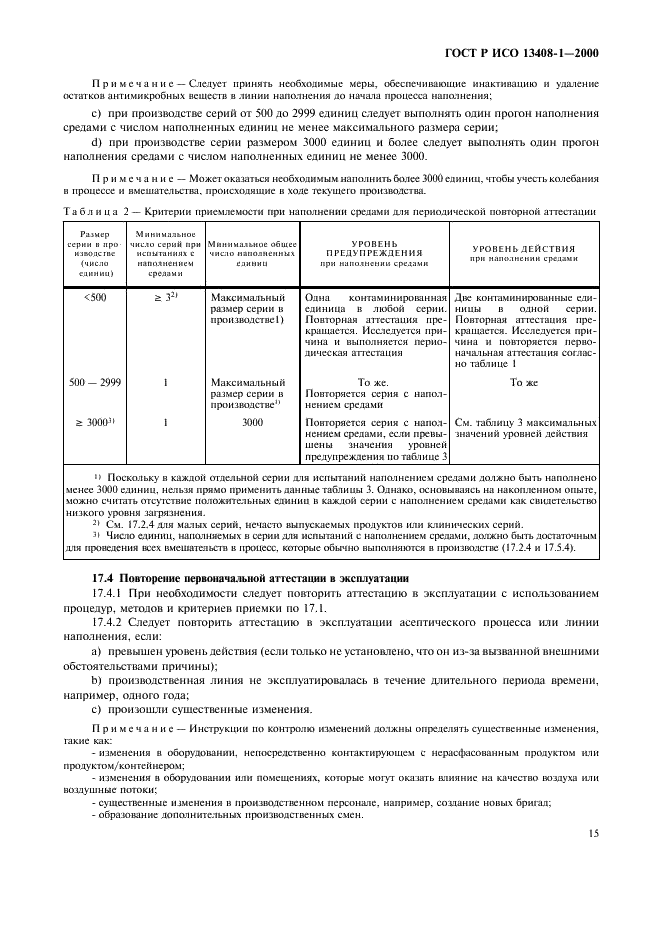
Страница 16

Страница 17
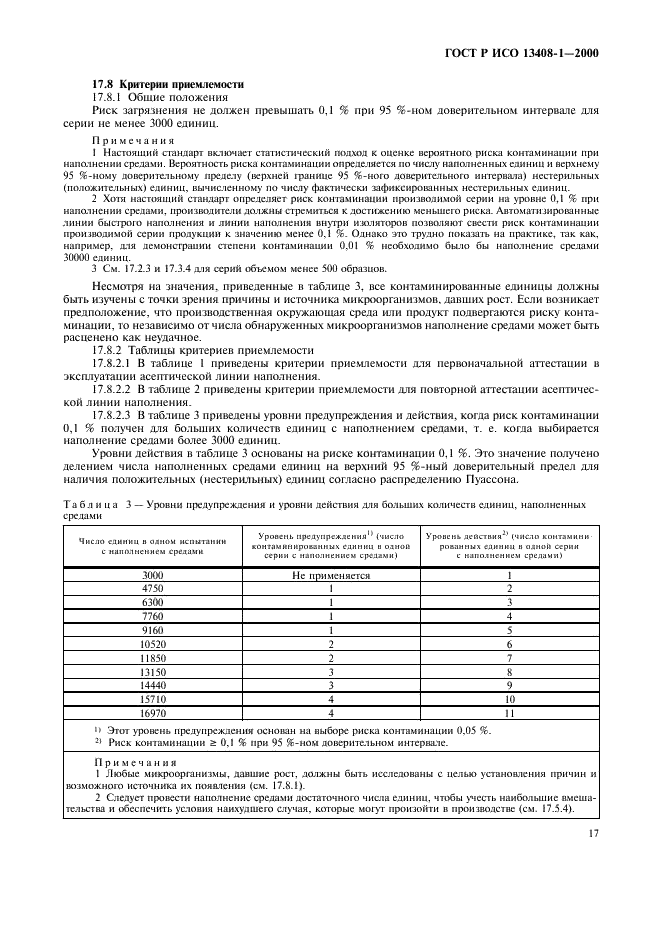
Страница 18

Страница 19

Страница 20

Страница 21

Страница 22

Страница 23

Страница 24

Страница 25

Страница 26
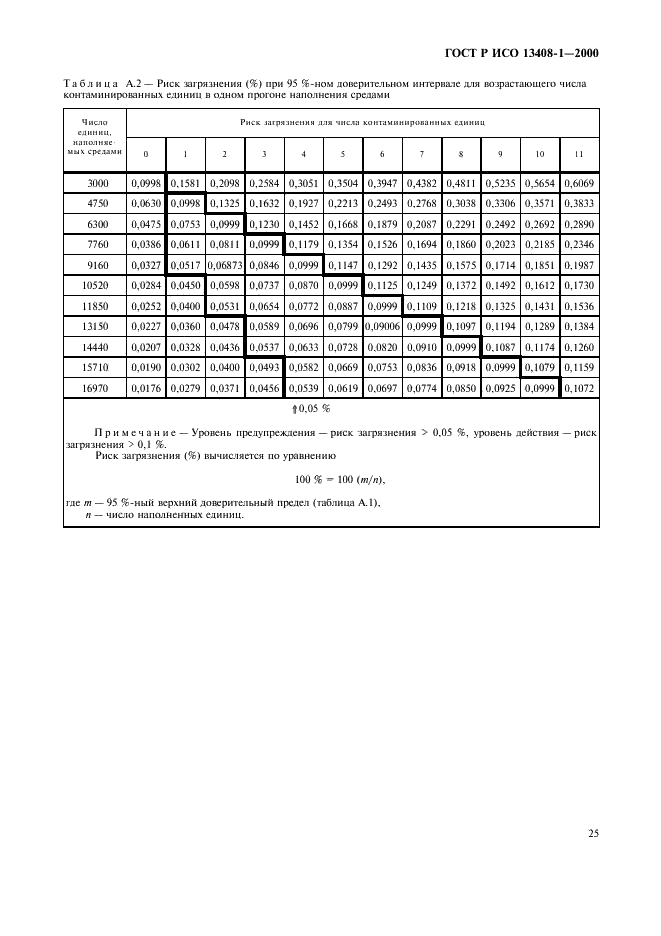
Страница 27

Страница 28

Страница 29

Страница 30

Страница 31

Страница 32
ГОСТ Р ИСО 13408-1-2000 ГОСУДАРСТВЕННЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
АСЕПТИЧЕСКОЕ ПРОИЗВОДСТВО МЕДИЦИНСКОЙ ПРОДУКЦИИ
Часть 1
Общие требования
Издание официальное
БЗ 7 -2000/203
ГОССТАНДАРТ РОССИИ Москва
ГОСТ Р ИСО 13408-1-2000
Предисловие
1 ПОДГОТОВЛЕН Ассоциацией инженеров по контролю микро загрязнений (АСИНКОМ)
ВНЕСЕН Техническим комитетом по стандартизации ТК 383 «Стерилизация медицинской продукции* Госстандарта России
2 ПРИНЯТ И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Госстандарта России от 25 сентября 2000 г. № 232-ст
3 Настоящий стандарт содержит аутентичный текст международного стандарта ИСО 13408-1—98 «Асептическое производство медицинской продукции. Часть I: Общие требования»
4 ВВЕДЕН ВПЕРВЫЕ
& ИПК Издательство стандартов, 2000
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Госстандарта России
II
ГОСТ Р ИСО 13408-1-2000
Содержание
1 Область применения………………………………………………. I
2 Определения…………………………………………………….I
3 Система управления качеством………………………………………..3
4 Персонал……………………………………………………….4
5 Проектирование помещений………………………………………….5
6 Зоны асептического производства………………………………………6
7 Вспомогательные зоны за пределами зоны асептического производства……………..7
8 Системы вентиляции и кондиционирования воздуха и контроля………………….7
9 Переодевание……………………………………………………8
10 Очистка и дезинфекция зоны асептического производства……………………..9
11 Аттестация оборудования, используемых средств и валидация процесса…………….9
12 Материалы и оборудование, поступающие в зону асептическою производства……….. 10
13 Производство……………………………………………………10
14 Программа контроля окружающей среды…………………………………. 11
15 Уровни предупреждения и действия…………………………………….12
16 Исследования и отчеты……………………………………………..12
17 Наполнение средами (имитация процесса наполнения)………………………..13
IS Контроль стерильности готового продукта…………………………………19
19 Обработка паром на месте……………………………………………20
20 Фильтрация в технологическом процессе………………………………….20
21 Лиофилизация……………………………………………………21
Приложение А Расчет риска контаминации для данного числа единиц, наполненных средами . 24 Приложение В Библиография…………………………………………..26
III
ГОСТ Р ИСО 13408-1-2000
Введение
Медицинская продукция, на этикетке которой указано «Стерильно*, должна быть изготовлена соответствующими валидироваиными методами. Технический комитет ИСО/ТК 198 подготовил стандарты по финишной стерилизации (стерилизации п упаковке) медицинской продукции радиацией (ГОСТ Р ИСО 11137-2000), влажным теплом (ГОСТ Р ИСО 11134— 2000). жидкими химическими стерилизующими веществами (ИСО 14160—98) и оксидом этилена (ГОСТ Р ИСО 11135-2000). Если медицинская продукция должна быть стерильной, но не подлежать финишной стерилизации, используется асептическое производство. Существуют две ситуации, при которых используется асептическое производство:
a) асептическая подготовка растворов и наполнение ими;
b) асептические приготовление, перемещение и упаковка твердых продуктов, которые не подлежат финишной стерилизации в окончательной упаковке.
Асептическое производство требует предварительной стерилизации всех частей или компонентов продукции, которые находятся в прямом контакте с продуктом, упаковываемым в асептических условиях. Продукт производится в контролируемой окружающей среде, в которой загрязнение частицами и микроорганизмами не должно превышать определенных уровней и участие человека сведено до минимума.
Асептическое производство требует особой аккуратности и ответственности. В производстве используются вал иди рова иные системы, персонал, обученный соответствующим образом, контролируемые окружающие среды и полностью документированные технологические процессы.
В то время как при финишной стерилизации используются процессы с известной летальностью (эффективностью уничтожения микроорганизмов), стерильность в асептическом производстве может быть обеспечена только за счет помещений, оборудования и персонала, связанных с процессом. Следует также использовать данные о продукте, чтобы сохранить стерильность в контейнере и/или закрытой системе в соответствии с асептическими принципами.
Мри асептическом производстве учитывают следующие основные факторы:
a) обучение персонала:
b) планировочные решения и характеристики здания, помещений и оборудования;
c) программу контроля загрязнений частицами и микроорганизмами;
d) системы подготовки воды, пара, воздуха и других технологических газов;
e) описание технологических операций и инструкции по их выполнению, включая персонал, материалы, потоки материалов, подготовку растворов и соответствующие критерии приемки;
0 использование и валидацию процессов стерилизации, включая методы дезинфекции;
g) методы валидации и требования к имитаторам наполнения и системам контейнер/укупорка;
h) эксплуатационные инструкции по критериям приемки, исследовательские отчеты и решения по выпуску/отзыву продукта.
Стандарт ИСО 13408-1 был подготовлен Техническим комитетом ИСО/ТК 198 •Стерилизация медицинской продукции». ИСО 13408 «Асептическое производство медицинской продукции» состоит из следующих частей:
— Часть I: Общие требования
• Часть 2: Фильтрации
— Часть 3: Лиофшизация
— Часть 4: Стерилизация и очистка на месте
— Часть 5: Асептическое производство твердых медицинских изделий
— Часть 6: Иэалирукнцие/барьерные технаюгии
IV
ГОСТ Р ИСО 13408-1-2000 ГОСУДАРСТВЕННЫ Й СТАНДАРТ Р ОС С И Й С К О Й ФЕДЕ Р А Ц И И
АСЕПТИЧЕСКОЕ ПРОИЗВОДСТВО МЕДИЦИНСКОЙ ПРОДУКЦИИ
Часть 1
Общие требования
Aseptic processing of health tare products.
Part 1. Genera! requirements
Дата введения 2002—01—01
1 Область применения
Настоящий стандарт устанавливает общие требования к процессам, программам и процедурам валидации и контроля в асептическом производстве медицинской продукции.
Примечание — Последующие части стандарта будут посвящены специальным вопросам асептического производства, включая детализированное описание различных специфических процессов и методов, относящихся к фильтрации, лиофилизации. стерилизации и очистке на месте, изолирующей технологии и производству твердых медицинских изделий.
Настоящий стандарт не заменяет требования национальных регламентов, таких как Правила надлежащего производства — Good Manufacturing Practice (GMP) и/или руководства, которые относятся к сфере определенной национальной или региональной юрисдикции.
2 Определения
В настоящем стандарте используют следующие термины с соответствующими определениями:
2.1 уровень действия (action level) «контроль окружающей среды*: Установленный уровень загрязнения микроорганизмами или частицами, при превышении которого требуется немедленное вмешательство и корректирующие действия.
2.2 уровень действия (action level) «наполнение средами»: Установленный уровень или число нестерильных проб при наполнении средами (имитации наполнения), при превышении которого необходимо исследовать причину нестерильиости и выполнить корректирующие действия.
2.3 уровень предупреждения (alert level) «контроль окружающей среды»: Установленный уровень загрязнения микроорганизмами или частицами, который дает раннее предупреждение о потенциальной тенденции отклонения от нормальных эксплуатационных условий, при котором не требуется обязательное определенное корректирующее действие, но может потребоваться проведение исследования причин такого отклонения.
2.4 уровень предупреждения (alert level) «при работе с наполнением средами»: Установленный уровень или число нестерильных проб при наполнении средами (имитации наполнения), при достижении которого необходимо установить причину нестерильиости. но выполнять определенные корректирующие действия необязательно.
2.5 асептическое наполнение (aseptic filling): Часл. асептического процесса, при котором предварительно стерилизованный продукт наполняется и/или он упаковывается в стерильные контейнеры и укупоривается.
2.6 линия асептического наполнения (aseptic filling line): Технологическое оборудование или установка, где в асептических условиях проводится наполнение контейнеров и/или медицинских изделий.
Примечание — Обычно линия асептического наполнения строится так. что процесс наполнения контейнеров и/или медицинских изделии проходит вдоль линии (отсюда термин «линия»).
И мание официальное
I
ГОСТ Р ИСО 13408-1-2000
2.7 асептическое проиюодство (aseptic processing): Асептическое наполнение контейнеров для продукта и/или упаковка изделий в контролируемой окружающей среде, в которой обеспечение воздухом, материалами, оборудованием и персоналом регулируется гак, чтобы загрязнение микроорганизмами и частицами не выходило за устано&аенные пределы.
2.8 зона асептического производства — ЗАЛ (aseptic processing area — АРА): Контролируемая окружающая среда для асептического производства, состоящая из нескольких зон. в которых обеспечение воздухом, материалами, оборудованием и персоналом регулируется так. чтобы загрязнение микроорганизмами и частицами не выходило за установленные пределы.
2.9 протокол изготовления серии — партии (batch manufacturing record): Производственная документация. которая свидетельствует, что серия или партия продукта изготовлена в соответствии с установленным технологических» процессом и требованиями к обеспечению качества.
2.10 бионагрузка (bioburden): Популяция живых микроорганизмов на медицинском продукте или упаковке до стерилизации.
2.11 биопагрузка (bioburden): Популяция живых микроорганизмов на материалах и оборудовании, поступивших в зону асептического производства (ЗАМ).
2.12 биологический индикатор (biologoeal indicator): Готовый к применению инокулированный носитель в первичной упаковке, обеспечивающий определенную резистентность (устойчивость) к конкретному режиму стерилизации.
Примечание — Микроорганизмы часто используются на носителе, который представляет собой материал подложки с находящимися на нем тест-организмами.
2.13 форма контейнера (container configuration): Конструкция контейнера независимо от емкости.
II р и м с ч а н и е — Поскольку не все продукты, изготовляемые в асептических условиях, могут иметь контейнер в качестве окончательной упаковки, в настоящем стандарте также используется выражение «форма продукта/контейнера».
2.14 критическая производственная зона (critical processing zone): Локальная зона в асептическом производстве, в которой продукт и поверхности, контактирующие с продуктом, открыты в окружающую среду.
Примечание — Асептические операции, выполняемые в критической производственной зоне, могут включать асептические соединения, наполнение, надевание пробок и укупорку.
2.15 критическая поверхность (critical surfaces): Поверхность в критической производственной зоне, находящаяся в непосредственной близости к асептическим операциям и представляющая риск для продукта.
2.16 перепад давления (differential air pressure): Разность давлений между помещениями или зонами или внутри них.
2.17 дезинфицирующее средство (disinfectant): Химический или физический агент, который инактивирует вегетативные микроорганизмы, но необязательно высокорезистивные споры.
2.18 микрофлора окружающей среды (environmental Нога), и зол яты окружающей среды: Микроорганизмы. присутствующие в технологической или производственной среде и/или выделенные в ней.
2.19 газовый фильтр (gas filter): Пористый материал, устанавливаемый в линию со сжатым воздухом с целью удаления неживых и/или живых частиц из газовых потоков, которые идут прямо или косвенно в зону контакта с продуктом.
2.20 медицинская продукция — продукт (health care product): Медицинские изделия, лекарственные средства (фармацевтические или биологические) и диагностические средства «in vitro».
2.21 высокоэффективный фильтр очистки воздуха по частицам (high efficiency particulate air filter), ПЕРА фильтр — ХЕПА фильтр: Устройство, в котором с помощью фильтрующего материала осуществляется отделение аэрозольных частиц от фильтруемого воздуха с минимальной эффективностью 99.97 % (что соответствует коэффициенту проскока 0,03 %) для частиц с размером 0.3 мкм СЮР (дноктнлфталат) — аэрозоля или другого предусмотренного документацией аэрозоля.
2.22 ламинарный поток воздуха (laminar air flow): Поток воздуха, в котором скорости воздуха вдоль параллельных линий тока одинаковы.
Примечание — Ламинарный поток части используется в ламинарных шкафах и укрытиях.
См. также олнонапраазенный поток (2.33).
2.23 наполнение средами — имитация наполнения (media fills): Метод оценки асептического процесса с использованием питательной среды для микроорганизмов.
Примечание — Наполнение средами — это синоним имитации процесса для контроля, имитатора наполнения продуктом, имитации процесса наполнения, питательного бульона для испытаний, наполняемого питательного бульона и т. д.
2
ГОСТ Р ИСО 13408-1-2000
2.24 другие производственные зоны (other processing zones): Производственные юны. не относящиеся к критическим производственным зонам, в которых медицинские продукты не открыты для окружающей среды.
Примечание — Эти зоны включают юны подготовки, транспортирования и хранения стерилизованных компонентов, контейнеров и балк-продукта (нсрасфасованного продукта — «ангро») в защитной таре; выгрузочные зоны автоклавов и производственные помещения, из которых производится доступ в критические зоны.
2.25 контактная поверхность продукта (product contact surfaces): Поверхность, которая приходит в контакт со стерилизованным продуктом или контейнером/укупоркой.
2.26 стерилизующий фильтр для продукта (product sterilizing filter): Пористый материал с номинальным размером пор 0,22 мкм, способный удерживать определенное количество микроорганизмов при определенных условиях и с использованием определенных методов контроля.
2.27 аттестация (qualification): Документированный исследовательский пронесс, используемый изготовителем медицинской продукции, чтобы удостовериться в надежности и свойствах оборудования и/или процесса, проводимый до их приемки к использованию в производстве.
Примечание— Аттестация оборудования и/или процессов обычно включает в себя аттестацию установленного оборудования (после монтажа), аттестацию в ос пашенном состоянии, аттестацию в эксплуатации.
2.27.1 аттестация установленною оборудования (installation qualification): Процесс, который показывает, что установка или процесс калиброваны и соответствуют всем относящимся к ним проектным критериям и стандартам безопасности.
2.27.2 аттестация в оснащенном состоянии (operational qualification): Комплекс проверок, который демонстрирует, что оборудование и/или процесс функционируют как предусмотрено, существуют инструкции по эксплуатации оборудования и персонал обучен включать, управлять и обслуживать оборудование.
2.27.3 аттестация в эксплуатации (performance qualification): Комплекс проверок системы, доказывающий ее эффективность и воспроизводимость.
2.28: смена (shift): Плановый период работы или производства, продолжительность которого обычно не превышает 12 ч, в котором занята одна и та же группа работников.
2.29 стерильный (sterile): Состояние, свободное от живых микроорганизмов.
П р и м с ч а н и с — На практике не существует абсолютно надежного способа доказательства отсутствия живых микроорганизмов (см. 2.30).
2.30 стерилизация (sterilization): Валидированный процесс, обеспечивающий отсутствие живых микроорганизмов в продукте.
Примечание — Число микроорганизмов, которые выживают после процесса стерилизации, может быт ь выражено в вероятностном виде. Вероятность может быть снижена до очень малою значения, но никогда не может быть снижена до нуля.
2.31 вспомогательные зоны вне зоны асептического проишодства 3AII (support areas outside АРА):
Зоны с контролем окружающей среды, не находящиеся внутри асептической зоны производства и не являющиеся частью критической или иной производственной зоны.
2.32 финишная стерилизация (terminal sterilization): Процесс, при котором продукт стерилизуется в окончательной упаковке и который позволяет проводить измерения и количественную оценку летальности микроорганизмов.
2.33 однонаправленный поток воздуха (unidirectional air Пои): Поток воздуха, линии тока которого имеют одно направление и который может облачать или не обладать одинаковыми скоростями струй воздуха по ходу течения параллельных линий тока.
См. также ламинарный поток воздуха (2.22).
2.34 вентиляционный фильтр (vent filter): Пористый материал, способный удерживать живые и неживые частицы из газов, входящих в закрытый объем и выходящих из него.
3 Система управления качеством
Для того, чтобы обеспечить контроль за всеми действиями, апияющими на асептическое производство, должна быть организована система управления качеством, соответствующая характеру выполняемых операций. Если не применяются заменяющие это понятие национальные, региональные или международные Правила надлежащего производства — Good Manufacturing Practice, система
3
ГОСТ Р ИСО 13408-1-2000
управления качеством должна соответствовать требованиям ГОСТ Р ИСО 9001 и/или ГОСТ Р ИСО 9002 |5, 6|.
Примечание —В дополнение к требованиях! к продукции, компонентам и произволе!иенным регламентам система управления качеством может включать письменные инструкции и требования в отношении:
a) условии окружаюшей среды в зоне асептическою производства;
b) очистки и дезинфекции зоны асептического производства;
c) стерилизации продукта, оборудования и системы контейнер/укупорка:
d) асептического производства бал к-продукта (нерасфасо ванного продукта), например лиофилизации, асептической кристаллизации, сушки порошков и т. д.;
е> перемещения различных предметов в зону асептического производства или критическую производственную зону;
О порядка переодевания персонала;
g> внутрипроизводственною контроля и оценки:
h) обучения операторов и технического персонала;
i) порядка контроля за изменениями:
j) валидации.
4 Персонал
4.1 Управление персоналом
4.1.1 Следует разработать и принять инструкции по эксплуатации асептического производства, включая обучение персонала и контроль.
4.1.2 Следует контролировать эффективность использования этих инструкций.
4.1.3 Управленческий персонал должен отвечать за соответствие обучения требованиям, необходимым для допуска персонала к работе в асептической зоне в соответствии с 4.2.
4.2 Обучение для аттестации на право работать в зоне асептического производства
4.2.1 Весь персонал, имеющий допуск в зону асептического производства, должен быть аттестован на соответствие требованиям 4.2.2 и 4.2.3. Обучение по различным дисциплинам и выполняемым работам следует проводить с учетом индивидуальных обязанностей и направлено на достижение требуемого уровня знаний.
4.2.2 Критерии опенки соответствия персонала должны быть отражены в учебных программах. Весь персонал, работающий в зонах асептического производства, в том числе занятый техническим обслуживанием, должен быть обучен следующему;
a) гигиене персонала, например, мытью рук и методам дезинфекции;
b) правилам, касающимся ювелирных изделий или применения косметики;
c) асептической технике, например, персонал, работающий в зоне асептического производства. должен избегать:
1) лишних движений и контактов с критическими поверхностями;
2) лишних движений и разговоров, которые могут вызвать генерацию частиц и турбулентность:
3) движений над открытыми контейнерами и открытым продуктом и компонентами;
4) создания препятствий движению воздуха над критическими поверхностями;
d) основам микробиологии;
e) процедурам переодевания (см. раздел 9);
0 производству стерильных продуктов внутри зоны асептического производства;
g) действиям по защите качества продукции в экстренных случаях, например, при отказах системы вентиляции и кондиционирования воздуха, системы энергоснабжения и пр.
4.2.3 Персонал, имеющий периодический доступ в зону асептического производства, включая руководителей, работников служб контроля и обеспечения качества, который имеет периодический доступ в зону асептического производства, должен быть обучен и аттестован в соответствии с 4.2.2 и должен быть обучен следующим основным вопросам:
a) гигиене персонала;
b) правилам, касающимся ювелирных изделий или применения косметики;
c) основным элементам асептической техники:
d) основам микробиологии;
0 процедурам переодевания.
4
ГОСТ Р И СО 13408-1-2000
Если с учетом строгих ограничений зоны асептического производства ото трудно осуществить на практике, то указанный персонал должен тщательно контролироваться опытными работниками.
4.2.4 Следует вести документацию о прохождении обучения и аттестации.
4.2.5 Весь персонал, который непосредственно принимает участие в операциях наполнения или производства стерильной продукции в критических зонах, должен принимать участие в испытаниях с использованием наполнения средами в соответствии с требованиями настоящего стандарта не менее одного раза в год.
4.2.6 Новый персонал, работающий в критических производственных зонах, должен принять участие не менее чем водном испытании с использованием наполнения средами или эквивалентной асептической операции, которая может производиться в учебной обстановке, до того как он будет допущен принять участие в работе, выполняемой в критических производственных зонах.
4.2.7 Весь персонал должен проходить повторное обучение в соответствии с документированными инструкциями как по выполняемым функциям, так и по соответствующим элементам системы обеспечения качеств;» с определенной периодичностью или при необходимости.
4.3 Общее состояние здоровья персонала
4.3.1 Персонал должен сообщать об изменениях сосгояния своего здоровья, которые могут повлиять на асептическое производство (воспаление, повреждения кожи, обычная простуда, понос и пр.).
4.3.2 При изменении состояния здоровья, влияющем на работу в асептическом производстве, работники не должны допускаться в критические производственные зоны, но могут работать в других зонах.
Примечание — Персонал, допускаемый для работы в асептических условиях, должен ироходигь первичное и периодическое медицинские обследования.
4.4 Конгроль персонала
4.4.1 Работники, обученные и аттестованные для работы в зоне асептического производства, должны проходить микробиологический контроль по соответствующей программе, которая включает отбор проб с одежды и перчаток.
Примечание — Общим правилом является проведение микробиологического отбора проб с одежды и перчаток после их использования.
4.4.2 Результаты этого контроля должны использоваться для обнаружения тенденций изменения контаминации и оценки необходимости повторного обучения персонала.
5 Проектирование помещений
5.1 Особенности проектирования помещений
При проектировании зон асептического производства нужно учесть следующие особенности планировочных решений и конструкций:
a) обеспечить приспособленность поверхностей стен, пола и потолка для очистки и их способность выдерживать обработку дезинфицирующими средствами;
b) зффективно герметизировать потолки:
c) избегать уступов и других горизонтальных поверхностей, на которых могут скапливаться частицы и которые могут нару шать потоки воздуха;
d) выполнять монтаж трубопроводов, воздуховодов и прочих коммуникаций гак, чтобы избежать образований труднодоступных мест или других поверхностей, трудно доступных для очистки;
e) предусматривать достаточно места для зон переодевания, хранения чистой и загрязненной одежды и мытья рук;
1) разделять зоны переодевания и подготовки от зоны асептического производства посредством воздушных шлюзов и передаточных камер для компонентов, материалов и оборудования:
g) учитывать характер потоков воздуха, которые могут поатнять на продукт и критические поверхности;
h) устанаашвать окна и другие средства наблюдения, где это нужно;
i) поддерживать соответствующий перепад давления воздуха между помещениями различных классов;
j) оборудовать воздушные шлюзы системами, исключающими нахождение обеих дверей в открытом состоянии:
к) поддерживать температуру и, если необходимо, относительную атажность в допустимых пределах и, по возможности, с непрерывным контролем;
5
ГОСТ Р И СО 13408-1-2000
I) располагать оборудование п зоне асептического производства таким образом, чтобы облегчить доступ к нему оператора и обслуживающего персонала и свести до минимума возможность сообщения открытых контейнеров и продукта с окружающей средой:
т) располагать оборудование, требующее частого вмешательства оператора или обслуживающего персонала, в удалении от критических производственных зон:
II) учитывать потенциальные источники перекрестного загрязнения.
Примечания
1 Особое внимание должно быть уделено выбору месга расположения зоны асептического производства относительно других зон в производственном здании. Обоснование выбора этого места должно быть документировано.
2 В зданиях многоцелевого назначения зону асептического производства следует располагать вдали от зон с интенсивными потоками транспорта (материалов, оборудования и персонала) или отделять ее физическими барьерами.
3 Если в зоне асептического произведены используются чувавительные вещества. цитотоксические или другие опасные материалы. то в проекте помещения эти особенности должны быть учтены.
5.2 Рассмотрение проекта помещений
5.2.1 Процесс рассмотрения проекта помещений должен быть проведен и документирован гак. чтобы показать соответствие проекта специфическим требованиям производства продукции. Проект помещения следует рассматривать также при введении новых процессов или видов продукции.
5.2.2 Для существующих устройств следует провести ретроспективный анализ этого требования.
5.3 Поток материалов
В проекте помещений, где располагается зона асептического производства, следует предусмотреть контроль за потоками компонентов и материалов, чтобы:
a) поддерживать микробнштогическую чистоту в критических производственных зонах;
b) минимизировать попадание загрязнений в зону асептического производства и обеспечить контроль загрязнений таким образом, чтобы не допустить их в критические производственные зоны:
c) исключить смешивание чистых и грязных предметов.
6 Зоны асептического производства
6.1 Общие положения
Примечание — Зона асептического производства состоит из зон. для которых требуется разделение и контроль. Требования к качеству воздуха в каждой зоне зависят от вида выполняемых операций. Эти зоны разделяются на критические производственные зоны и прочие производственные зоны.
6.1.1 Зона асептического производства должна представать собой контролируемое пространство. в котором загрязнение микроорганизмами и частицами находится в установленных пределах.
6.1.2 Доступ в зону асептического производства должен быть ограничен: в нее может входить только аттестованный персонап. как указано в 4.2.
6.1.3 Следует предусмотреть необходимый однонаправленный поток воздуха и/илн положительный перепад давления, чтобы не допустить попадания загрязнений в зону асептического производства из соседних зон.
6.1.4 Должна быть принята, документально оформлена, введена и поддерживаться программа контроля окружающей среды.
6.2 Кршические производственные зоны
6.2.1 Должны быть определены критические производственные зоны и документально установлены требования к допустимому загрязнению этих зон микроорганизмами и частицами.
6.2.2 Должны быть предприняты необходимые меры по сведению к минимуму возможности загрязнения стерилизуемых предметов, материалов или окружающей среды.
6.2.3 В 1 м3 воздуха критических производственных зон должно содержаться менее 3500 частиц размером 0,5 мкм и более в состоянии *в эксплуатации*.
Примечания
1 Качество воздуха должно соответствовать зоне А. классу 5 ИСО или классу ПК) в используемых национальных и международных стандартах по качеству воздуха.
2 Критические производственные зоны подлежат эффективному контролю во время эксплуатации с целью выявления тенденций изменения параметров окружающей среды.
3 Допускается, что не всегда возможно проводить контроль соответствия чистоты по частицам во время процесса наполнения из-за образования частиц или капелек от самого процесса.
6
ГОСТ Р ИСО 13408-1-2000
6.2.4 Критические производственные зоны подлежат текущему контролю на присутствие микроорганизмов, т. с. микрофлоры/изолятов в окружающей среде (14.3.1.1) и аэрозольных частиц (14.4).
6.3 Другие производственные зоны (виутри зоны асептического производства)
6.3.1 Должны быть определены другие производственные зоны и установлены требования к их загрязнению микроорганизмами и частицами.
6.3.2 Должны быть предприняты необходимые меры по сведению к минимуму возможности загрязнения стерилизуемых предметов, материалов или окружающей среды.
6.3.3 В 1 м3 воздуха других производственных зон должно содержаться менее 350000 частиц размером 0,5 мкм и более в состоянии 1в эксплуатации».
Примечание — Эю качество воздуха обычно соответствует зоне В, классу 7 ИСО или классу 10000 в используемых национальных и международных стандартах но качеству воздуха.
6.3.4 Другие производственные зоны подлежат текущему контролю на присутствие микроорганизмов. то есть микрофлоры/изолятов в окружающей среде (14.3.1.1) и аэрозольных частиц (14.4).
7 Вспомогательные зоны ia пределами зоны асептического производства
7.1 В 1 м3 воздуха вспомогательных зон должно содержаться менее 3500000 частиц размером 0,5 мкм и более (состояние «оснащенное» или «в эксплуатации» специфицируется в документации)*.
Примечания
1 Эго качество воздуха должно соответствовать Зонам С/ D, классам 7(8) ИСО или классам 1 0000 (100000) в используемых национальных и международных стандартах по качеству воздуха.
2 Дезинфекция и контроль окружающей среды ЭТИХ зон могут быть менее частыми, чем для производственных зон.
7.2 Вспомогательные зоны подлежат текущему контролю на присутствие микроорганизмов, то есть микрофлоры/изолятов в окружающей среде.
8 Системы вентиляции и кондиционирования воздуха и контроля
Примечание — Основные элементы системы вентиляции и кондиционирования воздуха и нрофаммы контроля требуют соответствующего подхода при проектировании и контроле асептических производственных зон, включая обеспечение относительной влажности, температуры, скорост и потока воздуха, высокоэффективной фильтрации, организации однонаправленных потоков воздуха и перепада да&чсиия между соседними помещениями.
8.1 Температура и относительная влажность
8.1.1 Значения температуры и. при необходимости, относительной влажности воздуха должны быть определены, контролироваться и регулироваться так. чтобы выполнялись требования комфорта сотрудников и качества продукта. Это прямо влияет на асептическую технологию и потенциальный уровень загрязнений.
8.1.2 Эти значения должны учитывать требования работающего персонала и эксплуатируемого оборудования.
8.2 Воздух
8.2.1 Перепад давления воздуха между соседними зонами должен быть специфицирован, контролироваться и регулироваться.
8.2.2 Во все критические производственные зоны должен подаваться воздух от Н ЕРЛ фильтров, скорость которого должна соответствовать требованиям установленного класса чистоты.
8.2.3 Скорость однонаправленного потока воздуха должна контролироваться для каждого НЕРА фильтра в соответствии с программой через определенные интервалы времени.
П р и м с ч а н и с — Значительное снижение скорости ногока воздуха может привести к увеличению -загрязнения.
8.2.4 Должны быть определены и документированы требования к потокам воздуха, чтобы показать соответствие потока воздуха технологическому процессу; следует провести исследования атияния турбулентности на эффективность очистки потоком воздуха.
7
1
В ИСО 13408-1 указано только состояние «в эксплуатации». В Правилах GMP ЕС рассматривается как состояние «в эксплуатации», так и «оснащенное» состояние. Это учтено в настоящем стандарте.
ГОСТ Р И СО 13408-1-2000
8.3 Целостность МЕРА фильтров
8.3.1 Се






